Contoh Soal Kimia Kelas X SMA – Kali ini quipper.co.id akan membahas tentang contoh soal kimia kelas x sma semester 1 beserta jawabannya. Download Sakura Live Mod Apk Streaming Bar Bar Parah 2022
Mari kita pelajari bersama soal dan juga pembahasannya yang telah quipper.co.id buat sebagai berikut dibawah ini.
Daftar Isi :
Pengertian Soal Kimia Kelas X SMA

Kimia ialah merupakan suatu cabang dari ilmu fisik yang akan mempelajari tentang sifat, struktur, susunan, dan juga perubahan materi.
Kimia kadang – kadang sering disebut juga dengan ilmu pengetahuan pusat karena untuk menjabani sebuah ilmu – ilmu pengetahuan alam, termasuk juga dengan fisika, geologi, dan juga biologi.
Soal Pilihan Ganda Kimia Kelas X SMA
Jawablah Dengan Benar Soal – Soal Sebagai berikut Dibawah Ini!
1. Apabila unsur – unsur disusun dengan menurut kenaikan massa atom relatifnya, ternyata unsur yang ke 8 ini menunjukkan persamaan sifat dengan unsur yang ke 1, unsur yang ke 9 ini juga menunjukkan persamaan sifat dengan unsur yang ke 2 dan seterusnya.
Pernyataan ini ditemukan oleh?
A. A.R. Newland.
B. D.I. Mendeleev.
C. J.W. Dobereiner.
D. Lothar Meyer.
E. Wilheim Rontgen.
2. Pertama kali yang mengemukakan suatu sistem periodik yang ada dalam bentuk tabel ialah?
A. J.W. Dobereiner.
B. A.R Newland.
C. D.I. Mendeleev.
D. Lothar Meyer.
E. Wilheim Rontgen.
3. Pernyataan yang tidak benar ialah yang mengenai suatu sistem periodik dalam bentuk panjang ialah?
A. Terdiri atas 7 periode.
B. Terdiri atas 8 golongan A.
C. Periode 1 terdiri atas 2 unsur.
D. Golongan IIA terdiri atas 18 unsur.
E. Antara golongan IIA dan golongan IIIA terdapat unsur transisi.
Baca Juga : Latihan Soal Biologi Kelas 7 SMP
4. Unsur – Unsur yang terletak pada golongan IA disebut juga dengan?
A. Alkali.
B. Alkali tanah.
C. Halogen.
D. Transisi.
E. Gas mulia.
5. Unsur – Unsur berikut ini yang memiliki sifat yang mirip yaitu, kecuali?
A. H.
B. He.
C. Ne.
D. Ar.
E. Kr.
6. Unsur yang tidak termasuk dalam alkali tanah ialah?
A. Be.
B. Mg.
C. Ca.
D. S.
E. Ba.
7. Kelompok unsur yang terletak pada periode ke 3 ialah?
A. Li, C, dan O.
B. Mg, Ca, dan Al.
C. Al, Si, dan Cl.
D. Be, Na, dan Mg E. Li, Na, dan K.
Baca Juga : Soal Fisika Kelas 7 SMP/MTS
8. Unsur – Unsur gas mulia didalam sistem periodik ini terletak pada golongan?
A. IA.
B. IIA.
C. VIIIA.
D. IB.
E. VIIIB.
9. Unsur – Unsur yang ada didalam satu golongan memiliki?
A. Proton yang sama.
B. Elektron yang sama.
C. Elektron valensi yang sama..
D. Jari – Jari atom yang sama.
E. Jumlah kulit yang sama.
10. Unsur – Unsur yang ada dalam satu periode memiliki?
A. Proton yang sama.
B. Elektron yang sama.
C. Elektron valensi sama.
D. Jari – Jari atom yang sama.
E. Jumlah kulit yang sama.
11. Suatu unsur dengan 3 kulit dan elektron valensi 5 pada sistem periodik unsur terletak dalam?
A. Golongan IIIA, periode 5.
B. Golongan VA, periode 3.
C. Golongan VIIIA, periode 5.
D. Golongan VA, periode.
E. Golongan VIIIA, periode 3.
12. Suatu unsur yang memiliki konfigurasi elektron 2 8 8 1. Yang ada didalam sistem periodik terletak pada?
A. Periode 1, golongan IVA.
B. Periode 4, golongan IVA.
C. Periode 4, golongan IA.
D. Periode 1, golongan IA.
E. Periode 2, golongan IVA.
13. Diketahui suatu unsur – unsur dengan nomor atom sebagai berikut 11Na, 19K, 13Al, 17Cl. Unsur yang memiliki jari – jari atom yang paling panjang ialah?
A. K.
B. Ca.
C. Cl.
D. Al.
E. Na.
14. Energi ionisasi ialah merupakan suatu unsur sifat yang menyatakan?
A. Energi minimum yang diperlukan untuk melepas satu elektron dari satu atom netral dalam wujud gas.
B. Energi minimum yang diperlukan untuk menarik satu elektron pada pembentukan ion negatif.
C. Energi yang dibebaskan untuk menarik satu elektron pada pembentukan ion negatif.
D. Besarnya kecenderungan menarik elektron pada satu ikatan.
E. Besarnya kecenderungan menarik elektron membentuk ion negatif 15. Unsur Mg memiliki nomor atom 12 dan unsur P memiliki nomor atom.
15. Pernyataan yang tidak tepat untuk kedua unsur tersebut ialah?
A. Kedua unsur tersebut terletak pada periode yang sama.
B. Jari – Jari atom Mg lebih panjang dari jari-jari unsur P.
C. Energi ionisasi unsur P lebih besar dari energi ionisasi unsur Mg.
D. Afinitas elektron unsur P lebih besar dari afinitas elektron unsur Mg.
E. Ke elektronegatifan unsur Mg lebih besar dari keelektronegatifan unsur P.
16. Di antara unsur – unsur 3 Li, 9 Be, 11Na, 15P, dan 19K yang memiliki suatu energi ionisasi yang terbesar ialah?
A. Li.
B. Be.
C. Na.
D. P.
E. K.
17. Pernyataan yang tidak tepat untuk unsur – unsur yang terletak didalam satu golongan dari atas ke bawah ialah?
A. Energi ionisasi bertambah.
B. Jari – Jari atom bertambah.
C. Sifat logam bertambah.
D. Afinitas elektron berkurang.
E. Ke elektronegatifan bertambah.
18. Unsur – Unsur yang terletak pada satu periode dari kiri ke kanan yaitu?
A. Energi ionisasi bertambah.
B. Jari – Jari atom bertambah.
C. Sifat logam bertambah.
D. Afinitas elektron berkurang.
E. Ke elektronegatifan berkurang.
19. Jari – Jari atom unsur Li, Na, K, Be, dan B secara acak (tidak berurutan) dalam satuan angstrom (Å) adalah 2,01; 1,23; 1,57; 0,80; dan 0,89 maka jari jari atom K sama dengan ….
A. 0,80
B. 0,89
C. 1,23
D. 1,57
E. 2,01
20. Grafik yang menggambarkan suatu kecenderungan sifat unsur dalam satu golongan ialah?
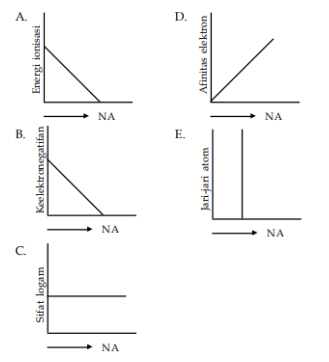
21. Diketahui nomor atom H = 1, C = 6, N = 7, O = 8, P = 15 dan Cl = 17 Senyawa berikut ini mengikuti aturan oktet, kecuali?
A. CHCl3.
B. NH3.
C. H2O.
D. CH4.
E. PCl5.
22. Unsur X yang memiliki nomor atom = 20 Unsur Y yang memiliki nomor atom = 9 Senyawa yang terbentuk dari kedua unsur ini memiliki rumus?
A. XY.
B. X2Y.
C. XY2.
D. X2Y3.
E. XY3.
23. Nomor dari atom unsur P, Q, R, dan S ialah 6,9,11, dan juga 18. Pasangan unsur – unsur yang dapat membentuk suatu ikatan ion ialah?
A. P dan Q.
B. S dan R.
C. Q dan S.
D. R dan Q.
E. P dan S.
24. Unsur X juga memiliki struktur atom dengan 1 elektron yang berada di kulit luarnya dan unsur Y juga memiliki afinitas elektron yang besar maka ikatan X-Y ialah merupakan ikatan?
A. Ion.
B. Kovalen koordinasi E. kovalen.
C. Homopolar.
D. Semipolar.
25. Ikatan antaratom mencakup?
A. Ikatan atom.
B. Ikatan nonlogam.
C. Ikatan kovalen.
D. Ikatan van der Waals.
E. Ikatan hidrogen.
26. Ke elektronegatifan H, Br, dan F masing – masing 2,1; 2,8; dan 4,0. Deret senyawa berikut ini yang tersusun didalam urutan kepolaran meningkat ialah?
A. BrF, HF, HBr.
B. HF, BrF, HBr.
C. BrF, HBr, HF.
D. HBr, HF, BrF.
E. HBr, BrF, HF.
27. Pasangan senyawa berikut ini yang merupakan pasangan senyawa yang memiliki suatu ikatan kovalen ialah?
A. KCl dan HCl.
B. H2 S dan Na2 S.
C. PCl3 dan FeCl3.
D. CH4 dan NH3.
E. H2O dan Na2O.
28. Unsur A yang bernomor atom 38 bersenyawa dengan unsur B yang bernomor atom 53. Senyawa dan ikatan yang terbentuk ialah?
A. A2B, kovalen.
B. AB2 , kovalen.
C. A2B3 , kovalen.
D. A2B, ion.
E. AB2 , ion.
29. Suatu Deret dari senyawa berikut ini yang tergolong senyawa kovalen, kecuali?
A. Hf, Hci, Hi.
B. BH3 , BF3 , CO2.
C. H2O, NH3 , CO2.
D. Li2O, CaO, MgO.
E. IF5 , CCl4 , CIF3.
30. Empat unsur M, N, Q, dan R dengan nomor atom berturut -turut 6, 11, 17, dan 19. Pasangan unsur yang dapat membentuk ikatan kovalen nonpolar ialah?
A. M dan R.
B. N dan R.
C. N dan Q.
D. M dan Q.
E. Q dan R.
31. Ikatan kovalen koordinasi yang terdapat pada?
A. H2o.
B. Nh4+.
C. Ch4.
D. Hf.
E. C2h4
32. Rumus elektron valensi molekul nitrometana digambarkan sebagai berikut Pasangan elektron ikatan yang menyatakan suatu ikatan kovalen koordinasi ialah?
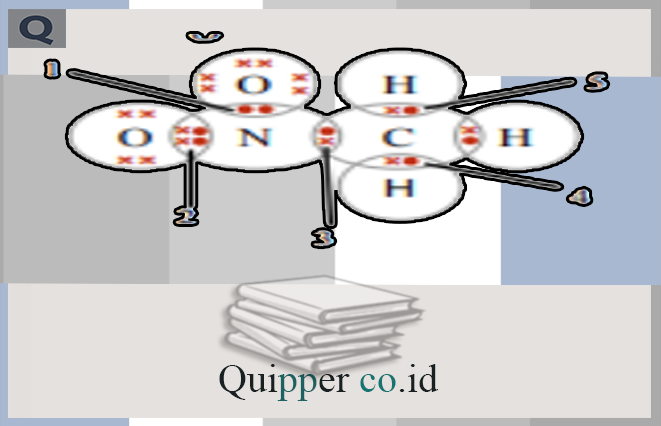
A. 1
B. 2
C. 3
D. 4
E. 5
33. Berdasarkan dengan no diatas, pasangan elektron ikatan yang menyatakan suatu ikatan kovalen rangkap ialah?
A. 1
B. 4
C. 3
D. 2
E. 5
34. Partikel dasar dalam atom terdiri atas?
A. Proton, elektron, dan positron.
B. Proton, neutron, dan nukleon.
C. proton, elektron, dan neutron.
D. Positron, nukleon, dan elektron.
E. Neutron, nukleon, dan elektron.
35. Berikut ini yang membuktikan model atom Thomson tidak tepat ialah sebagai percobaan?
A. Sinar katode.
B. Hamburan sinarα pada lempeng tipis emas.
C. Spektrum atom hidrogen.
D. Tetes minyak milikan.
E. Sinar kanal.
36. Kesimpulan bahwa muatan elektron –1,60 × 10–19 C diperoleh dari tetesan minyak dikemukakan oleh?
A. Sir Humphry.
B. Robert Milikan.
C. J.J. Thomson.
D. James Chadwick.
E. Willliam Crookes.
37. Pada hakikatnya percobaan Rutherford ialah?
A. Penemuan proton.
B. Penemuan neutron.
C. Penemuan inti atom.
D. Penemuan elektron.
E. Penemuan positron.
38. Notasi yang benar untuk proton, elektron, dan neutron dengan berturut – turut ialah?
A. 111 +1 -11 P; e; n.
B. 110 +1 -11 P; e; n.
C. 101 +1 -10 P; e; n.
D. 111 +110 P; e; n.
E. 101 +1 -10 P; e; n.
39. Pasangan yang merupakan isoton ialah atom – atom?
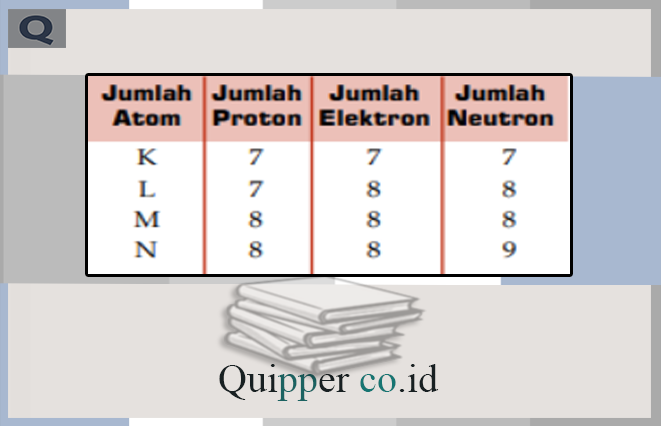
A. K dan L.
B. K dan M.
C. L dan M.
D. L dan N.
E. M dan N.
40. Kelemahan penyusunan atom dengan teori oktaf ialah?
A. Ada atom yang memiliki massa yang lebih tinggi dari urutan yang lebih rendah.
B. Karena urutan kenaikan suatu massa atom itu tidak kontinu.
C. Beberapa unsur yang menurut hitungan terdapat pada suatu kelompok, tetapi sifatnya tidak sama.
D. Penyusunan berdasarkan kenaikan massa atom banyak kelemahannya.
E. Sistem oktaf hanya berlaku pada unsur dengan nomor massa kecil.
41. Berikut ini merupakan ciri yang ditunjukkan oleh sistem periodik unsur modern, kecuali?
A. Terdapat 18 golongan.
B. Golongan terbanyak berisi 9 unsur.
C. Periode terbanyak berisi 32 unsur.
D. Terdapat 8 periode.
E. Terdapat golongan transisi luar dan transisi dalam.
42. Kelompok unsur dengan nomor atom berikut ini yang memiliki elektron valensi sama ialah?
A. 12, 20, 38, 56.
B. 12, 19, 38, 53.
C. 11, 18, 37, 52.
D. 13, 18, 31, 38.
E. 14, 18, 30, 39.
43. Pernyataan yang benar mengenai keteraturan sifat periodik dalam satu periode ialah?
A. Dari kiri ke kanan afinitas elektron bertambah besar.
B. Dari kiri ke kanan jari – jari atom akan semakin besar.
C. Dari kiri ke kanan potensial ionisasi semakin besar.
D. Dari kiri ke kanan keelektronegatifan semakin kecil.
E. Dari kiri ke kanan afinitas elektron semakin kecil.
44. Di antara ion poliatomik berikut ini yang berupa kation ialah?

45. Senyawa dengan rumus molekul berikut ini yang terdapat ikatan rangkap dua ialah?
A. Cl2.
B. N2.
C. NH3.
D. CH4.
E. C2H4.
46. Volume hidrogen yang bergabung dengan 24 liter oksigen untuk menghasilkan uap air ialah?
A. 24 liter.
B. 22,4 liter.
C. 48 liter.
D. 12 liter.
E. 44,8 liter.
47. Sebanyak 10 cm3 dan hidrokarbon tepat ber reaksi dengan 50 cm3 dan oksigen menghasilkan 30 cm3 karbondioksida.
Jika volume gas diukur semua pada suhu dan tekanan yang sama, rumus hidrokarbon tersebut ialah?
A. CH4.
B. C2H6.
C. C3H4.
D. C3H6.
E. C3H8.
48. Volume gas oksigen pada STP yang bereaksi dengan 12,8g gas SO2 untuk membentuk gas SO3 (Ar S = 32 ; O = 16) ialah?
A. 1,12 L.
B. 2,24 L.
C. 3,36 L.
D. 4,48 L.
E. 5,6 L.
49. Suatu oksida logam M tersusun atas 60 gram logam M (Ar = 60) dan 24 g oksigen (Ar = 16). Rumus empiris oksida logam tersebut ialah?
A. MO.
B. M2O3.
C. MO2.
D. M3O2.
E. M5O2.
50. Suatu molekul terbentuk dari unsur C dan H yang memiliki Mr 30 dan mengandung 70% massa C.
Senyawa tersebut ialah merupakan …. (Ar C = 12, H = 1).
A. CH4.
B. C2H4.
C. C3H5.
D. C2H6.
E. C3H6.
Soal Essay Kimia Kelas X SMA
1. Jelaskan gagasan teori atom dalton itu seperti apa?
2. Apakah yang dimaksud dengan energi ionisasi?
3. Apa yang dimaksud dengan jari – jari atom?
4. Bagaimana jari – jari dalam satu golongan dan satu periode? Jelaskan!
5. Dalam satu golongan, afinitas elektron dari atas ke bawah maka semakin? Jelaskan!
Kunci Jawaban Soal Kimia Kelas X SMA
Pilihan Ganda Contoh Soal Kimia Kelas X SMA
| 1. C | 11. B | 21. E | 31. B | 41. D |
| 2. B | 12. C | 22. C | 32. A | 42. C |
| 3. D | 13. B | 23. B | 33. B | 43. A |
| 4. A | 14. A | 24. D | 34. C | 44. D |
| 5. A | 15. E | 25. B | 35. B | 45. E |
| 6. D | 16. D | 26. E | 36. B | 46. C |
| 7. C | 17. A | 27. D | 37. C | 47. E |
| 8. C | 18. A | 28. A | 38. E | 48. B |
| 9. C | 19. E | 29. D | 39. C | 49. B |
| 10. E | 20. A | 30. D | 40. E | 50. D |
Essay Contoh Soal Kimia Kelas X SMA
| 1. Teori atom dalton ialah merupakan teori yang paling tua untuk mengenai penjelasannya tentang atom. Dalton menjelaskan bahwasannya atom ialah merupakan suatu zat yang tidak akan bisa di bagi – bagi lagi. Materi ini terdiri atas atom yang tidak dapat di bagi lagi. Semua atom dari unsur kimia yang tertentu dan memiliki massa dan sifat yang sama. |
| 2. Energi ionisasi (IE) ialah merupakan suatu energi yang di perlukan untuk mengeluarkan suatu elektron dari tiap mol spesies dalam keadaan gas. |
| 3. Jari – Jari atom ialah merupakan suatu jarak, dari inti atom ke orbital elektron yang terluar dan stabil didalam suatu atom agar keadaannya setimbang. Biasanya jarak ini diukur didalam satuan pikometer maupun angstrom. Di karenakan elektron – elektron senantiasa bergerak, maka dari itu untuk mengukur jarak dari inti atom sangat sulit. |
| 4. Dalam satu golongan, jari – jari atom ini makin ke bawah makin besar karena kulit yg di miliki oleh atom makin banyak, sehingga kulit akan terluar makin jauh dari inti. Satu golongan, makin ke bawah semakin besar jari atomnya sedangkan satu periode makin ke kanan semakin kecil juga jari atomnya karena proton dan elektron yg dimilkinya banyak. |
| 5. Dalam satu golongan dari atas ke bawah afinitas elektron makin kecil. sebab gaya tarik intinya semakin lemah maka atom tersebut semakin sulit untuk menangkap elektron yang akan mengakibatkan makin sedikit juga energi yang di bebaskannya. |
Akhir Kata
Terima kasih atas perhatian kalian semuanya semoga apa yang telah quipper.co.id bahas diatas dapat bermanfaat dan menjadi wawasan untuk kalian semuanya Aamiin.
