Materi makalah pelajaran yang akan admin sampaikan pada kesempatan kali ini adalah tentang pelajaran ilmu kimia senyawa dan Rumus Kimia Amonium Sulfat.
Ini adalah salah satu pelajaran ilmu kimia yang umumnya sering kita dapatkan disekolah dan berbagai pendidikan atau universitas lainnya.
Dengan mengetahui unsur lengkap dengan pengertian, sifat dan fungsi dari materi senyawa ini, tentunya ini akan mempermudah kita untuk lebih memahami tentang apa itu Amoniun Sulfat.
Nah biar sobat bisa lebihpaham betul mengenai materi pelajaran Rumus Kimia Amonium Sulfat ini, simak penjelasan selengkapnya seperti yang sudah admin sediakan di bawah ini.
Daftar Isi :
Apa Itu Amonium Sulfat?
Amonium sulfat yang memiliki rumus kimia (NH4)2SO4, merupakan garam anorganik yang memiliki beberapa kegunaan, misalnya sebagai pupuk untuk menyuburkan unsur hara tanah atau sebagai bahan tambahan pangan. Amonium sulfat mengandung 21% unsur nitrogen dan 24% unsur belerang.
Amonium sulfat terurai ketika dipanaskan hingga 250 ° C, pertama-tama membentuk amonium bisulfat. Jika dipanaskan sampai suhu yang lebih tinggi, amonium sulfat dapat terurai menjadi amonia. sulfur dioksida, nitrogen, dan air.
Rumus Amonium Sulfat
(NH4)2SO4
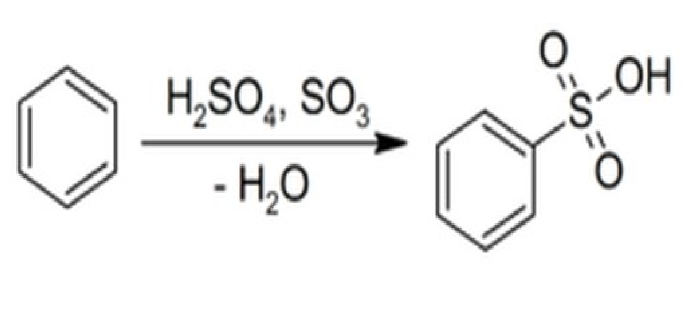
Pembuatan Amonium Sulfat
Pembuatan Amonium Sulfat dalam Proses Fase Gas-Cair Amonia dan Asam Sulfat (Proses Netralisasi) secara umum dibagi menjadi empat tahap, yaitu:
- persiapan bahan baku
- Fase reaksi netralisasi
- Tahap pemisahan dan pengeringan
- dan akhirnya pengemasan
Reaksi Kimia dari Asam Sulfat
- Membuat HCl dengan memanaskan H2SO4 pekat dengan natrium klorida
- H2SO4 + NaCl ==> NaHSO4 + HCl
Selain NaCl, pemanasan logam klorida dengan asam sulfat pekat dan mangan dioksida dapat menghasilkan HCl.
- Pembuatan SO3 dilakukan dengan memanaskan sejumlah besar asam sulfat pekat, yaitu P2O5.
- H2SO4 + P2O5 ==> SO3 + 2HPO3
- Pembuatan SO2 di laboratorium biasanya dilakukan dengan mereaksikan H2SO4 pekat dengan Cu.
- Baca Juga Proses Mitosis Cu + 2H2SO4 ==> CuSO4 + SO2 + 2H2O
- Pemanasan CaF2 dengan asam sulfat pekat di laboratorium dapat menghasilkan HF.
- CaF2 + H2SO4 ==> 2HF + CaSO4
- HI juga dapat dibuat dengan memanaskan garam NaI dengan H2SO4 pekat.
- 2NaI + H2SO4 ==> 2HI + Na2SO4
- Selain metanol, semua alkohol lain ketika bereaksi melepaskan molekul air. Metanol bereaksi dengan H2SO4 menghasilkan dimetil sulfat.
- 2CH3OH + H2SO4 ==> (CH3)2SO4 + H2O
- Asam sulfat akan menyerap etilen (C2H4) ketika di udara membentuk etil hidrogen sulfat C2H5.HSO4. C2H4 + H2SO4 ==> C2H5.HSO4
Fungsi Amonium Sulfat
Penggunaan utama amonium sulfat adalah sebagai pupuk untuk tanah alkalin. Di dalam tanah, ion amonium dilepaskan dan membentuk keseimbangan yang menurunkan pH tanah, menghasilkan sejumlah besar asam, sementara nitrogen berkontribusi lebih penting bagi pertumbuhan tanaman.
Kerugian utama menggunakan amonium sulfat adalah kandungan nitrogen yang rendah dibandingkan dengan amonium nitrat, yang meningkatkan biaya transportasi.
Ini digunakan sebagai bahan pembantu pertanian untuk penyemprotan insektisida, herbisida atau fungisida yang larut dalam air. Ada yang berfungsi untuk mengikat kation besi dan kalsium yang ada dalam sel air dan juga pada tumbuhan. Ini sangat efektif sebagai bahan pembantu untuk herbisida 2,4-D (amina), glifosat dan glufosinat.
Amonium Sulfat akan menutupi defisit belerang jangka pendek pada tanaman dan padang rumput, persyaratan kualitas tanaman, atau persyaratan pemeliharaan belerang padang rumput.
Granular amonium sulfat sangat penting sehingga direkomendasikan untuk kondisi subur dan untuk budidaya, pengisian silo dan pengeboran benih. Ini digunakan di Cropmaster, 31 putaran dan 36 putaran gabungan.
Berbagai fungsi dari Amonium Sulfat adalah sebagai berikut ini :
Fungsi Asam Sulfat Dalam Industri
- Asam sulfat dapat digunakan sebagai proses pembuatan deterjen.
- Industri manufaktur HNO3 menggunakan asam kuat.
- Pembuatan baterai untuk industri otomotif dapat menggunakan asam sulfat.
- Asam sulfat dapat digunakan sebagai proses untuk menghilangkan pengotor dalam proses penyulingan minyak.
- Pembuatan bahan peledak menggunakan asam sulfat sebagai reagen.
- Asam sulfat digunakan sebagai bahan baku pembuatan pupuk superfosfat dan amonium sulfat.
- Pembuatan rayon dengan asam sulfat.
- Asam sulfat digunakan untuk membuat perekat.
- Pembuatan pewarna dapat menggunakan asam sulfat.
- Asam sulfat dapat digunakan dalam proses pembersihan untuk pengolahan besi dan logam serta baja melalui proses plating.
Fungsi Asam Sulfat Bagi Kehidupan Sehari-Hari
- Sebagai bahan pembuatan pupuk.
- Menjadi cairan elektrolit baterai.
- Rumus kimia asam sulfat dapat digunakan dalam pembersih karat.
Contoh Soal Rumus Molekul
200 g senyawa organik memiliki massa molekul relatif = 180, senyawa ini terdiri dari 40% karbon, 6,6% hidrogen dan sisanya adalah oksigen. Diketahui Ar.C = 12, Ar.H = 1 dan Ar.O = 16. Kemudian tentukan rumus molekul senyawa tersebut.
- CH2O)n
- (Ar C x n) + (2.Ar H x n) + (Ar.O) = Mr senyawa
- 12n + 2n + 16n = 180
- 30n = 180
- n = 6
Jadi rumus molekulnya adalah C6H12O6.
Contoh soal 2
Coba perhatikan dan tentukanlah rumus molekul senyawa dengan rumus empiris CH jika Mr senyawa tersebut adalah 78?
Menjawab
Senyawa Sr = (CH)n
78 = (12 + 1)n
78 = 13n
n = 6
jadi rumus molekul senyawa tersebut adalah (CH)n = C6H6.
Akhir Kata
Demikian yang bisa admin quipper.co.id sampaikan tentang pelajaran ilmu Rumus Kimia Amonium Sulfat, semoga apa yang sudah admin sampaikan kali ini dapat bermanfaat bagi sahabat semua.
